Het veranderen van iemands genetische programmering is eenvoudiger dan je zou denken. Terwijl technieken voor het veranderen van DNA op moleculair niveau steeds breder worden gebruikt, is het ook mogelijk om eenvoudig genen in of uit te schakelen zonder het onderliggende genetische materiaal permanent te veranderen. Dat betekent dat we de genetische instructies die naar het lichaam van een organisme worden gestuurd, kunnen beïnvloeden door de omgeving of met medicijnen te veranderen.
Dit veld van 'epigenetica' helpt artsen al om te begrijpen hoe bepaalde ziekten werken, waarom lichaamsbeweging zo gunstig kan zijn en hoe we het verouderingsproces kunnen veranderen. Maar mijn collega's en ik proberen de rol van epigenetica in bacteriën te onderzoeken.
We hebben onlangs een mogelijke manier onderzocht om bacteriële epigenetica te beïnvloeden die mogelijk infecties kan stoppen zonder antibiotica te gebruiken. En gezien het feit dat veel bacteriën resistent worden tegen bestaande antibiotica, zou dat een vitale nieuwe manier kunnen zijn om ziekten te behandelen.
In onze studie werd gekeken naar de bacterie Acinetobacter baumannii, een belangrijke oorzaak van de infecties die mensen in ziekenhuizen kunnen oplopen en die tot 70 procent van de mensen die ermee besmet zijn, doodt. Antibiotica werken niet langer op sommige stammen van A. baumannii - en de Wereldgezondheidsorganisatie heeft het onlangs gerangschikt als de grootste bacteriële bedreiging voor de menselijke gezondheid.
We hebben al een aantal zogenaamde antivirulentiemedicijnen die geen bacteriën doden maar ze onschadelijk maken, zodat het immuunsysteem van het lichaam ze kan verwijderen zonder achter te laten om resistent te worden tegen het medicijn. Het bedenken van een manier om de epigenetica van bacteriën te beïnvloeden en de insecten onschadelijk te maken, kan ons helpen nieuwe antivirulentiemedicijnen te maken die een enorme bijdrage aan de geneeskunde zouden leveren.
Om dit proces te starten hebben we ons eerst tot menselijke epigenetica gewend. De meest voorkomende manier om onze epigenetica te beïnvloeden, is door een klein moleculair label aan ons genetisch materiaal toe te voegen dat een verwant gen in- of uitschakelt. In het bijzonder kunnen we een label dat bekend staat als een acetylgroep toevoegen aan een belangrijk eiwit dat histon wordt genoemd.
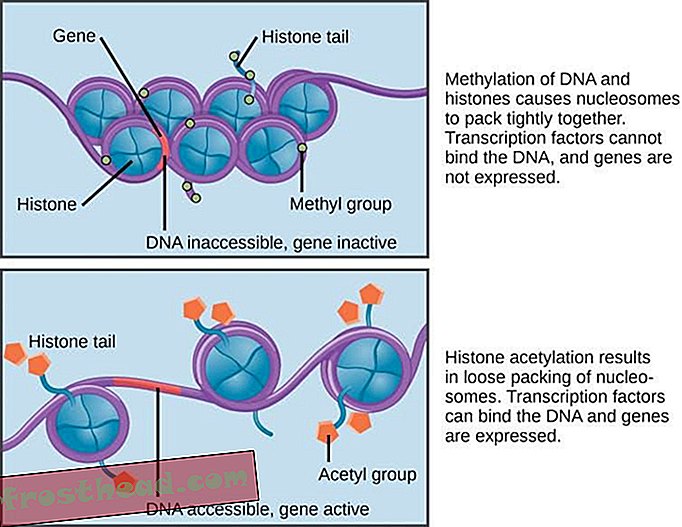 Een acetyl-tag toevoegen aan histone (CNX OpenStax, CC BY)
Een acetyl-tag toevoegen aan histone (CNX OpenStax, CC BY) Histone organiseert onze 2m lange DNA-moleculen zodat ze netjes in onze 100 micrometer lange cellen passen. Het toevoegen van de acetyl-tag is een natuurlijk mechanisme dat door cellen wordt gebruikt om de manier te veranderen waarop histon met DNA interageert. Het toevoegen van de acetyl-tags activeert normaal bepaalde genen, wat betekent dat ze het gedrag van de cel veranderen. Falen in dit histon-modificatieproces zijn gekoppeld aan kanker, hart- en vaatziekten en veel neurodegeneratieve aandoeningen.
Bacteriële cellen hebben hun eigen versie van histon, bekend als HU, die hun DNA organiseert en betrokken is bij het laten werken van al zijn functies. Bacteriën die "Gram-positief" worden genoemd, zoals die in ons spijsverteringsstelsel die ons helpen voedsel af te breken, kunnen niet overleven zonder HU te werken. En "gramnegatieve bacteriën", die meestal ziek zijn zoals Salmonella enterica, worden veel minder schadelijk zonder HU.
Nieuwe medicijnen
In onze studie hebben we vastgesteld dat het toevoegen van een acetyl-tag aan HU de manier waarop het in wisselwerking stond met het DNA aanzienlijk beïnvloedde. Dit betekent dat het zeer waarschijnlijk is dat een dergelijke aanpassing epigenetische veranderingen aanbrengt, die van invloed zijn op hoe de bacteriën groeien en andere organismen infecteren. Dus als we medicijnen kunnen maken die deze veranderingen in bacteriële eiwitten op deze manier aanbrengen, kunnen we een nieuwe manier hebben om infecties te stoppen.
Dit is op dit moment een heel belangrijke uitdaging in de geneeskunde, omdat bacteriën die resistent zijn tegen antibiotica wereldwijd 700.000 mensen doden. Als we geen nieuwe behandelingen vinden, kan het jaarlijkse dodental stijgen tot 10 miljoen in 2025.
Zodra we het verband tussen specifieke epigenetische veranderingen en bacteriële infecties hebben geverifieerd, kunnen we op zoek gaan naar stoffen die de epigenetica van bacteriën op deze manier veranderen om het minder schadelijk te maken. Er zijn al verschillende moleculen die zich op vergelijkbare wijze richten op humane epigenetica onder preklinische ontwikkeling of in klinische proeven. Dus een medicijn dat het vermogen van bacteriën om infecties te veroorzaken "uitschakelt" is misschien niet te ver weg.
Dit artikel is oorspronkelijk gepubliceerd op The Conversation.
Yu-Hsuan Tsai, docent organische chemie, Cardiff University

