In de laatste week van maart in 2009 kregen twee kinderen in Zuid-Californië griep. Ze waren 9 en 10 jaar oud, een meisje en een jongen, en hoewel het erg laat was in het griepseizoen, hadden ze allebei symptomen van het leerboek: plotselinge koorts, hoesten en een last van een vrachtwagen. De kinderen hadden geen band met elkaar - hun families woonden in aangrenzende provincies in de bodem van de staat - maar toevallig namen beide klinieken waar hun ouders hen mee namen deel aan griepvolgprojecten uitgevoerd door de Centers for Disease Control en Prevention, het Amerikaanse federale agentschap dat ziektebedreigingen thuis en over de hele wereld bewaakt.
Dat was een gelukkig ongeval, omdat het betekende dat beide kinderen hun keel afwisselden, om te controleren welke van de verschillende griepspanningen die elk jaar circuleren hen ziek maakte. Maar wat een routinematige eerste stap leek, werd al snel een bron van alarm. De twee kinderen, die meer dan 100 mijl uit elkaar woonden, hadden stammen die erg op elkaar leken - maar het was een nieuw type griep en gebaseerd op genetisch bewijs, het was afkomstig van varkens. Een griepstam die uit een diersoort springt om mensen te infecteren, is een signaal voor problemen; een virus dat het menselijk immuunsysteem nog nooit heeft meegemaakt, zal eerder ernstige ziekten en de dood veroorzaken.
Minder dan twee weken nadat de testresultaten binnenkwamen, verklaarden de Verenigde Staten een nationale noodsituatie voor de volksgezondheid. De soort verspreidde zich snel over de hele wereld en paniek volgde. In juni, toen wereldwijd gevallen opkwamen, verklaarde de Wereldgezondheidsorganisatie dat een grieppandemie - de eerste van de 21ste eeuw - was begonnen.
Bijna zodra de monsters werden geanalyseerd, kon de CDC de nieuwe stam isoleren en gebruiken als basis voor een noodvaccin. Maar griepvaccin-technologie is tientallen jaren oud en onhandig en het nieuwe virus werkte niet mee, reproduceerde slecht en vertraagde het omslachtige proces. De hele zomer en in de herfst vielen angstige ouders en artsen kinderartsen en geneesmiddelenfabrikanten aan, smekend om vaccin dat nog niet bestond. De eerste doses werden pas in oktober bekendgemaakt, nadat tienduizenden in de Verenigde Staten ziek waren geworden en 60 kinderen waren overleden. Het aantal door artsen gemelde gevallen piekte eind oktober. Tegen januari was er eindelijk genoeg vaccin om iedereen in het land te beschermen die normaal gevaccineerd zou worden, bijna 120 miljoen doses. Maar het publiek had interesse verloren en meer dan een kwart van het haastig gemaakte vaccin - ter waarde van honderden miljoenen dollars - werd vernietigd.
De varkensgriep van 2009 bleek niet het grote gevaar te zijn dat de gezondheidsautoriteiten vreesden. Miljoenen mensen werden wereldwijd ziek, maar hun ziektes waren grotendeels mild. Tussen 151.700 en 575.400 mensen stierven - maar hoewel dat een groot aantal lijkt, was het vergelijkbaar met een gemiddeld griepseizoen. De grootste impact was niet op leven en gezondheid, maar op het vertrouwen van het publiek in griepvaccins. De aflevering eindigde met gezondheidsinstanties die nieuwe inspanningen deden om de manier waarop griepprikken worden gemaakt en verspreid fundamenteel te veranderen.
En nu kunnen ze een glimp van een kans hebben.
**********
Een vaccin voor alle seizoenen
Ter bescherming tegen toekomstige griepepidemieën gaan onderzoekers verder dan het gebruikelijke schot in de arm. - Onderzoek door Sonya Maynard

 (Matthew Twombly)
(Matthew Twombly) 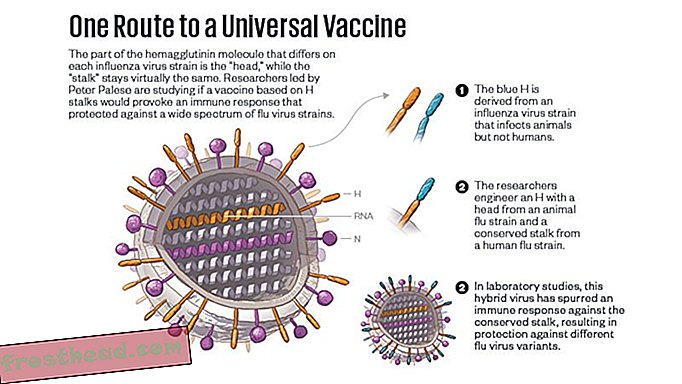 (Matthew Twombly)
(Matthew Twombly)  (Matthew Twombly)
(Matthew Twombly) In de laatste dagen van juni van dit jaar verzamelde een falanx van influenza-wetenschappers van over de hele wereld zich in een strakke, glazen ommuurde conferentieruimte in een doodlopende straat in een buitenwijk van Maryland. Ik was de enige verslaggever die aanwezig was op deze alleen-uitnodigende bijeenkomst, georganiseerd door de National Institutes of Health. De assemblage had meer in gedachten dan het versnellen van de vaccinafgifte. Het doel was om te onderzoeken of griepprikken volledig konden worden herleefd, van een formule die elk jaar opnieuw werd geschreven en afgeleverd tot een formule die om de tien jaar of zelfs een of twee keer in je leven kon worden gegeven: een universeel vaccin.
Anthony Fauci, de directeur van het National Institute of Allergy and Infectious Diseases, opende de bijeenkomst met de titel 'Pathway to a Universal Flu Vaccine'.
"De huidige seizoensgriepvaccins zijn niet consistent effectief, " vertelde hij de ongeveer 175 aanwezigen. “Het vaccin tegen mazelen, bof en rodehond is 97 procent effectief; vaccin tegen gele koorts is 99 procent effectief. [Griepvaccin] kan oplopen tot 10 procent. ”In het griepseizoen dat eindigde in het voorjaar van 2017, zei hij, had het vaccin ziekte voorkomen bij slechts 42 procent van de mensen die het gebruikten.
Die cijfers kunnen als een verrassing komen, als je bedenkt hoe agressief de volksgezondheid het griepvaccin aanmoedigt. De CDC beveelt aan dat elke inwoner van de VS die 6 maanden of ouder is en geen allergie voor een van de ingrediënten heeft, het vaccin elk griepseizoen moet ontvangen, en elk jaar produceren fabrikanten maar liefst 166 miljoen doses om aan die vraag te voldoen. Je kunt in het najaar niet naar een supermarkt of een drogisterij lopen zonder dat je wordt aangespoord om de foto te maken. Enorme werkplekcampagnes vragen werknemers om het in te nemen, en scholen adverteren het vaccin voor kinderen die pasgeborenen of kwetsbare grootouders kunnen infecteren, maar ook zelf ziek kunnen worden.
Juist vanwege de onvoorspelbaarheid van griep duwen autoriteiten het griepvaccin zo hard. Het mazelenvirus dat nu in de wereld circuleert, is hetzelfde als het virus dat 10 jaar geleden bestond, of 20 of 50. Maar griep verandert van seizoen tot seizoen, omdat het zich reproduceert en voortdurend kleine fouten maakt in zijn genetische code. De virussen floreren in het koude weer en fietsen elke lente en herfst heen en weer over de evenaar. Terwijl een nieuw griepseizoen zich afspeelt, analyseren planners de circulerende virussen om te voorspellen wat er zou kunnen gebeuren wanneer de ziekte weer op weg is naar de andere pool, en schrijven een bijpassende vaccinformule.
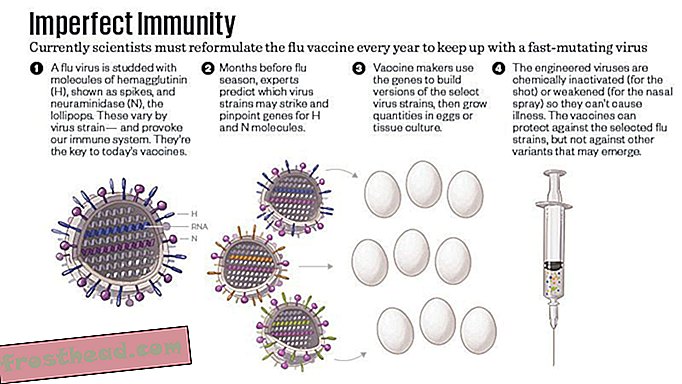
De productie van griepvaccins is een langzaam proces. De virussen die planners selecteren als de beste weergave van wat eraan komt - er zijn er meestal drie en in sommige formules vier - worden in een medium geplaatst waarmee ze zich in grote hoeveelheden kunnen reproduceren. (Historisch gezien gebruikten vaccinontwikkelaars miljoenen bevruchte kippeneieren, maar nu incuberen ze soms de virussen in in cellen gekweekte cellen van dieren of insecten.) Vervolgens deactiveren ze het virus, voor het injecteerbare vaccin, of verzwakken het voor de neusspray. Het kan zes maanden duren om voldoende virus te kweken en een vaccin te testen en te verpakken. In die tijd kan de rusteloze veranderlijkheid van griep de spanning van een seizoen in een richting sturen die niemand had verwacht, waardoor de bescherming die de planners hadden gehoopt toen ze de vaccinformule een half jaar eerder schreven, afnam.
Volgens de CDC sterven elk jaar in de Verenigde Staten tussen de 12.000 en 56.000 mensen aan griep en worden er tot 710.000 meer ziek genoeg om in het ziekenhuis te worden opgenomen. Die aantallen omvatten mensen die het vaccin weigeren, en degenen die het niet kunnen nemen vanwege allergieën voor een van de componenten ervan. Maar ze omvatten ook mensen die waren gevaccineerd maar uiteindelijk niet werden beschermd omdat het circulerende virus niet aan de verwachtingen voldeed.
Dat is de tol in de gemiddelde jaren, wanneer het virus zichzelf net voldoende heeft veranderd - "drift" is de technische term - om van fabrikanten te eisen dat ze de vaccinformule van het voorgaande jaar enigszins aanpassen. Maar een paar keer per eeuw, over onvoorspelbare tijdsverschillen, zweeft het virus niet, maar verschuift het naar een vorm die zo nieuw is dat het bestaande vaccin geen basis is voor een nieuwe en eerdere infectie geen afweer biedt. Wanneer zo'n griep op gang komt, is het resultaat een pandemie.
De griep van 1918 was de moeder van alle grieppandemieën. Maar er waren ook pandemieën in 1968 en 1957, die elk ten minste een miljoen mensen doodden - en, op basis van historische verhalen maar zonder microbiologie om ze te bevestigen, in 1889, 1847, 1830, 1781, en zo ver terug als een epidemie van "hijgende onderdrukking" in 1510. Het griepvirus werd pas in 1933 in het laboratorium geïdentificeerd en het eerste vaccin werd in 1945 gelicentieerd.
"We hebben zeker een beter vaccin nodig, dat in grote lijnen beschermend is en veel langer meegaat", zegt Dan Jernigan, de directeur van de griepafdeling van de CDC, die het bureau vertegenwoordigde tijdens de NIH-bijeenkomst. "Hoe ver daar vandaan is, kan ik niet zeggen."
**********
Als je een griepvirus kunt doorsnijden, ziet het er ongeveer uit als een bal, bezaaid met moleculen die lijken op spikes en paddestoelen. De spikes zijn hemagglutinine, kortweg H of HA genoemd; de paddestoelen zijn neuraminidase, bekend als N of NA. Er zijn 18 subtypen hemagglutinine en 11 subtypen neuraminidase en influenza A-stammen (de stammen die pandemieën veroorzaken) zijn vernoemd naar de combinaties van de twee die ze herbergen. Het 1918-virus was een H1N1, 1957 was een H2N2, 1968 was een H3N2. (Binnen een bepaalde stam, zoals H1N1, kunnen na verloop van tijd verdere mutaties optreden, vooral wanneer een vogelvirus zijn weg vindt naar andere dieren zoals varkens.)
Hemagglutinine is het deel van het virus waarmee het zich kan binden aan de cellen in onze longen, om ze in kleine fabrieken te veranderen voor het maken van meer virussen. Omdat het zich op het oppervlak van het virus bevindt, reageren onze immuunsystemen eerst op hemagglutinine. Het probleem is dat het virus constant muteert. De antilichamen die we tegen hemagglutinine van dit seizoen produceren, zullen ons niet noodzakelijkerwijs beschermen tegen toekomstige griepspanningen.
Maar wat als een vaccin zou kunnen worden gemaakt van een deel van het virus dat nooit verandert?
"Dit is iets waar we misschien maar vijf jaar aan hebben kunnen denken", zegt Peter Palese, voorzitter van de microbiologie aan de Icahn School of Medicine op de berg Sinaï in New York City. "Inzicht in virale immunologie, en in het bijzonder de structuur van hemagglutinines, heeft ons laten nadenken over vaccinconstructies die een bredere immuunrespons zouden kunnen veroorzaken."
 Toen Peter Palese begin jaren zeventig Oostenrijk verliet, was er relatief weinig bekend over de genen die betrokken zijn bij griepvirussen. Palese ontwikkelde de eerste genetische kaart voor griepstammen A, B en C. (Bryan Derballa)
Toen Peter Palese begin jaren zeventig Oostenrijk verliet, was er relatief weinig bekend over de genen die betrokken zijn bij griepvirussen. Palese ontwikkelde de eerste genetische kaart voor griepstammen A, B en C. (Bryan Derballa) Palese is een van 's werelds meest vooraanstaande grieponderzoekers, met een lange lijst publicaties en patenten. De muren van zijn kantoor op de berg Sinaï, die uitkijkt op de East River en de start- en landingsbanen van LaGuardia Airport, zijn bekleed met ingelijste onderscheidingen en behaalde en eredoctoraten, beginnend met zijn doctoraat aan de Universiteit van Wenen in zijn geboorteland Oostenrijk. Hij bestudeert al meer dan vier decennia griep, stelt de eerste genetische kaarten van griepvirussen op en definieert de mechanismen van antivirale geneesmiddelen. Hij pionierde ook een methode voor het introduceren van mutaties in het genoom van griepvirussen, waardoor we kunnen begrijpen hoe ze ziekte veroorzaken.
De aankomst van Palese op de berg Sinaï in 1971 kwam slechts vijf jaar voordat een cluster van gevallen van griep optrad onder militaire rekruten in Fort Dix in New Jersey, op 75 mijl rijden van zijn laboratorium. De gevallen werden veroorzaakt door een varkensgriep; Palese was perfect geplaatst om de nationale paniek te zien terwijl federale experts voorspelden dat een pandemie zou ontstaan door de afwijkende stam, en een noodvaccin formuleerde. Hun voorspelling was verkeerd. Er was geen pandemie - maar er was een gelijktijdige uitbraak van tijdelijke verlamming, het Guillain-Barré-syndroom genaamd, bij meer dan 450 mensen die de opnames ontvingen. De vaccinatiecampagne werd afgeblazen te midden van chaos. De aflevering wierp jarenlang een hekel aan griepvaccinonderzoek, terwijl de cruciale behoefte aan een vaccin werd benadrukt dat niet opnieuw hoefde te worden gecreëerd wanneer een crisis dreigde.
Decennia lang leek een universele formule bijna ondenkbaar. Vervolgens, binnen een week in 2009, kondigden twee sets onderzoekers aan dat ze antilichamen hadden geïdentificeerd die niet aan de lollipopkop van de hemagglutinine maar aan de sticklike stengel ervan waren gehecht. Dit was opwindend, omdat de stengel van hemagglutinine in technische taal 'geconserveerd' is: het is in wezen hetzelfde van stam tot stam. De ontdekkingen wekten de hoop dat stamantilichamen niet slechts één virusstam, maar vele konden verslaan, en dat bleek waar te zijn. De onderzoeksteams onthulden dat de gevonden antilichamen bescherming boden tegen een aantal influenzavirusstammen.
Maar er was geen duidelijke manier om die hoop om te zetten in een vaccin. Stamantilichamen zijn zeldzaam omdat het immuunsysteem zo zelden een kans heeft om op de stengel te reageren; in zijn ontmoeting met griepvirus ontmoet het eerst de hemagglutininekop. Om de stam de basis van een vaccinstrategie te maken, zouden onderzoekers een soort operatie aan hemagglutinines moeten uitvoeren; in een manoeuvre zoals het slaan van een golfbal van een tee, zouden ze de hoofden van de moleculen uit de weg moeten bewegen.
In de jaren sinds die ontdekkingen hebben onderzoekers geprobeerd, maar slaagden er niet in om de kop met succes te verwijderen: een onthoofde stengel valt gewoon uit elkaar en antilichamen binden er niet aan. Er zijn ook veelbelovende resultaten, methoden om de stengel van de hemagglutinine te verankeren met gemanipuleerde nanodeeltjes of met ingeruilde aminozuren.
Palese en zijn lab hebben een andere strategie ontwikkeld. In 2013 hebben ze de kop van een H1-hemagglutinine verwijderd en vervangen door de kop van een hemagglutinine uit een afzonderlijke tak van de stamboom van het griepvirus - een stam die dieren maar geen mensen trof. (De onderzoekers ontwikkelden later een manier om deze deeltjes helemaal opnieuw te laten groeien, met de vreemde koppen al op hun plaats.) De vervanging was bedoeld om het immuunsysteem te leiden voorbij de nieuwe kop te springen alsof het niet bestond, en antilichamen te genereren tegen de stam in plaats daarvan. De strategie werkte. De chimere hemagglutinine veroorzaakte een immuunrespons en beschermde proefdieren tegen infecties. Een fase 1-proef is net begonnen voor menselijke proefpersonen.
"We hebben het gedaan bij muizen, bij cavia's, bij fretten - daar werkt het geweldig, " zei Palese. “Maar muizen zijn geen mannen; fretten zijn geen mensen. Het moet echt bij mensen worden getest. ”
**********
In 1997 kondigde een onderzoeksteam van het Walter Reed Army Medical Center aan dat het het virus dat de griep in 1918 veroorzaakte opnieuw tot leven zou wekken.
Wetenschappers hadden nooit kunnen verklaren wat deze pandemie zo gemeen maakte. Het eindigde lang voordat griepvirussen in laboratoria werden geïsoleerd. Historische verslagen getuigden van de snelle, dramatische manier waarop het zijn slachtoffers doodde, maar het virus zelf leek voorbestemd om een mysterie te blijven. Maar aan het einde van de 20e eeuw onthulden onderzoekers van het Armed Forces Institute of Pathology dat ze fragmenten van het virus hadden gevonden in een lang bewaard autopsiemonster, genomen van een soldaat die stierf in 1918.
Niemand in de hechte wereld van griepwetenschappers had met dit team van moleculaire pathologen aan grieponderzoek gewerkt. Het werd geleid door een patholoog, Jeffery K. Taubenberger, wiens prestaties omvatten het weer in elkaar zetten van een mazelenachtig virus dat een pod dolfijnen doodde. Nu, gewapend met het autopsiemonster van de gevallen soldaat, kreeg het team hulp van andere virologen - en van een gepensioneerde patholoog die op eigen initiatief naar Alaska ging om weefsels te nemen van een Inuit-slachtoffer wiens lijk in de toendra was ingevroren voor de afgelopen acht decennia. In 2005 voltooide de Taubenberger-groep de reconstructie van het gehele virus uit 1918 en de extractie van de genomische sequentie. De verbazingwekkende prestatie haalde krantenkoppen over de hele wereld. "Dat Jurassic Park, Frankenstein ding van het herrijzen van een moordenaarvirus - je kunt zien hoe dat interesse opwekte, " zegt Taubenberger. "Maar het werd niet gedaan alleen voor de gee whizz-factor."
 Jeffery Taubenberger verbaasde het publiek tien jaar geleden toen hij het griepvirus uit 1918 reconstrueerde uit segmenten die in lijken waren gevonden. Nu gebruikt hij wat hij heeft geleerd om een nieuw vaccin te bouwen. (Eli Meir Kaplan)
Jeffery Taubenberger verbaasde het publiek tien jaar geleden toen hij het griepvirus uit 1918 reconstrueerde uit segmenten die in lijken waren gevonden. Nu gebruikt hij wat hij heeft geleerd om een nieuw vaccin te bouwen. (Eli Meir Kaplan) Voor wetenschappers begon Taubenberger's werk aan het virus uit 1918 de zwarte doos te openen van wat het zo virulent maakte. Het hielp hen beter te begrijpen hoe griepvirussen zich aanpassen aan mensen, en wat er nodig is om moderne pandemieën te voorkomen. Het is niet eenvoudig om de NIH-campus te bezoeken; het vereist parkeren op een beveiligd terrein, het passeren van een lijn als een immigratiecontrole, je tas door een scanner duwen en je foto laten maken voor een tijdelijke ID. Om de wetenschapper te bezoeken die de griep uit 1918 deed herleven, is nog meer inspanning vereist. Mobiele telefoons worden weggehaald en opgesloten - bouwregels staan geen camera's toe - en Taubenberger zelf moet naar de lobby komen en een insigne vegen om je binnen te laten. Op de vloer waar hij werkt, bevinden zich geneste sets gesloten deuren, retinascanners, gecodeerd hangsloten op de vriezers en lagen van sterilisatiesystemen. Samen bevatten ze de dreiging van het gereconstitueerde virus en andere dodelijke virussen die een hoge mate van biocontainment vereisen.
Toen ik er was, was Taubenberger net verhuisd naar een klein, reserve kantoor dat uitkwam op rijen laboratoriumbanken en zuurkasten en couveuses. De meeste van zijn boeken en onderzoekspapieren lagen netjes opgeborgen in dozen op de vloer. Een ingelijste poster aan de zijkant adverteerde een uitvoering van een strijkkwartet dat hij meer dan twee decennia geleden schreef ('nr. 2 in G Major'). Taubenberger speelt hobo, Engelse hoorn, klarinet en piano, en hij leidde de ouverture naar zijn eerste operette aan de George Mason University toen hij 20 jaar oud was.
Nu, op 56-jarige leeftijd, is Taubenberger het hoofd van de afdeling virale pathogenese en evolutie van het National Institute of Allergy and Infectious Diseases, het NIH-agentschap dat Fauci leidt. Maar andere griepvaccinonderzoekers zien zijn achtergrond nog steeds als onorthodox en zijn benadering is heel anders dan die van Palese. "Ik heb niet geprobeerd een anti-stengelman te zijn, " vertelde hij me. “Ik denk dat immuniteit tegen stelen waarschijnlijk belangrijk zal zijn. Ik denk niet dat het de magische kogel is die andere mensen denken. '
Taubenberger's versie van een universele formule hangt in plaats daarvan af van zogenaamde "virusachtige deeltjes", kortweg VLP's. De FDA heeft al VLP's goedgekeurd voor vaccins tegen hepatitis B en HPV. De groep van Taubenberger bouwde op die modellen voort. Om hun eerste versie van een universeel vaccin te maken, gebruikten ze VLP's met hemagglutinines van vier verschillende griepstammen die pandemieën in het verleden hadden veroorzaakt, waaronder die in 1918. Ze combineerden vervolgens de vier soorten VLP's tot een 'cocktailvaccin', in de hoop het zou een bredere bescherming bieden dan seizoensgebonden vaccins.
Het construct werkte beter dan ze hadden verwacht. Bij muizen veroorzaakte het een beschermende immuunrespons tegen stammen die een van die vier hemagglutininen droegen - en tot hun verbazing ook tegen andere stammen die niet overeenkwamen met de subtypen van het vaccin. Taubenberger is openhartig over het feit dat hij nog niet begrijpt hoe zijn vaccin zo'n brede immuniteit oproept. "De vraag hoe het werkt om alle grieptypes te beschermen, " zei hij, "is iets waar we nog steeds aan werken."
Als een griepvaccin zou kunnen worden gemaakt om te beschermen tegen alle vormen van het virus, zou dit niet alleen een veel betere immuniteit bieden, maar ook het hele proces veranderen hoe we griepprikken toedienen. Het zou het mogelijk maken om vroeg in het leven één vaccin te geven, misschien met periodieke booster-shots op de weg. Het zou de druk decomprimeren om de kwetsbaren te vaccineren in de korte tijd voordat een nieuw griepseizoen begint.
Net als Palese zou Taubenberger graag zien dat een universeel griepprikje onderdeel wordt van het reguliere vaccinatieschema. Dat zou meer levens redden dan we waarschijnlijk beseffen, voegde hij eraan toe. Hoewel we pandemieën als de grote moordenaars beschouwen, bezetten ze in de 100 jaar sinds 1918 slechts ongeveer zes. "Met uitzondering van 1918, zijn er waarschijnlijk geen pandemieën geweest in de 20e eeuw, of begin 21e eeuw nu, die een impact hebben gehad die hoger was dan echt slechte seizoensgriepjaren, " zei hij. Volgens de CDC veroorzaakte de pandemie van 2009 meer dan 12.000 doden in de Verenigde Staten. "Seizoensgebonden flus, " zei Taubenberger, "hebben elk jaar gelijk in dat bereik."
**********
Een maand na de bijeenkomst in juni ontmoette ik Fauci in zijn NIH-kantoor. Hij is een immunoloog, met een speciale interesse in HIV - hij nam het bestuur van NIAID over in 1984, in de vroegste dagen van de AIDS-epidemie - en dat geeft hem een uniek inzicht in de problemen met het bereiken van broodnodige vaccins. Het was tenslotte in 1984 dat toenmalig secretaris van Volksgezondheid en Human Services Margaret Heckler verklaarde dat een vaccin tegen HIV kon worden bereikt "in ongeveer twee jaar". Dat is nog steeds niet het geval.
Sinds het begin van die epidemie zijn volgens de Wereldgezondheidsorganisatie ongeveer 35 miljoen mensen gestorven aan een hiv-infectie. Dat is ongeveer een derde van de geschatte tol van de grieppandemie van 1918, en die cijfers benadrukken hoe belangrijk een universeel vaccin zou zijn.
"Er zijn nog enkele wetenschappelijke problemen, " vertelde Fauci me. “Kunnen we echt een reactie opwekken die echt kruisbeschermend is tussen soorten? Ik denk dat het antwoord ja is - maar ik kan je niet vertellen dat we een echt universeel griepvaccin zullen krijgen, omdat ik niet zeker weet of we wetenschappelijk hebben bewezen dat we dat kunnen. 'Toch herhaalde hij:' We moeten ons eraan houden. Met een universeel griepvaccin zouden we pandemieën van de tafel kunnen nemen, in plaats van elke tien jaar onze staart achterna te jagen over een nieuwe vogelgriep of een nieuwe varkensgriep. Zo'n vaccin zou ons ook in staat stellen om het beter te doen met seizoensgriep, dus dat zou een twofer zijn. "
Voor nu blijven Palese en anderen zich concentreren op het induceren van stamantilichamen, terwijl de groep van Taubenberger blijft werken aan zijn cocktailbenadering, in de hoop om over ongeveer een jaar met menselijke proeven te beginnen. Andere groepen volgen verschillende strategieën. Eén benadering betreft een eiwit genaamd matrix 2, dat wordt gecodeerd op het RNA van het influenzavirus en het de inhoud ervan in een cel laat legen. Een andere methode is gericht op het activeren van T-cellen, die cellen doden die zijn geïnfecteerd met het virus.
Welke methode ook succesvol blijkt te zijn, en meer dan één zou hetzelfde kunnen zijn: een vaccin is niet alleen wetenschap. Het is ook regelgeving en productie en marketing. In die gebieden staat een universeel griepvaccin voor uitdagingen die volledig los staan van de wetenschappelijke. Het huidige, imperfecte griepvaccin levert wereldwijd meer dan $ 3 miljard op.
"De echte uitdaging is dat er al een gevestigde, en zeer volwassen, particuliere onderneming is die griepvaccin produceert met een systeem van jaarlijkse levering dat een bepaald bedrag garandeert, " zei Michael Osterholm, de oprichter van het centrum voor onderzoek naar en infectieziekten aan de Universiteit van Minnesota. “Hoe gaat u dat veranderen? Wie gaat dat betalen, aangezien de kosten van onderzoek en ontwikkeling kunnen betekenen dat het vaccin aanzienlijk duurder zal zijn dan we al hebben? Welk bedrijf zal dat omarmen? '
 "We moeten accepteren dat er een pandemie komt", schreef Michael Osterholm in een invloedrijk artikel in New England Journal of Medicine uit 2005. "Is er iets dat we kunnen doen om deze cursus te vermijden?" (Nate Ryan)
"We moeten accepteren dat er een pandemie komt", schreef Michael Osterholm in een invloedrijk artikel in New England Journal of Medicine uit 2005. "Is er iets dat we kunnen doen om deze cursus te vermijden?" (Nate Ryan) In 2012 bracht de organisatie van Osterholm een uitgebreid rapport uit waarin werd opgeroepen tot 'game-changing' griepvaccins. In dat rapport, en in een eerder dit jaar gepubliceerd boek, voerde Osterholm aan dat alleen het produceren van nieuwe formules in het laboratorium griepvaccinatie niet vooruit kan helpen. Hij voorziet zowel een door de overheid gefinancierd Manhattan-project als een filantropische inspanning om intensief onderzoek naar een nieuw vaccin te ondersteunen.
Als dat eenmaal is bereikt, wil hij dat de publieke en private sector een financiële garantie bieden aan productiebedrijven dat zij zullen profiteren van de overstap naar het nieuwe vaccin. "Totdat we dat doen, " zegt Osterholm, "griepvaccin is praktisch een weesgeneesmiddel." Met andere woorden, er is weinig stimulans voor farmaceutische bedrijven om te investeren in onderzoek en ontwikkeling.
Andere recente vaccininspanningen hebben niet voor dezelfde uitdagingen gezorgd. Twee jaar nadat Ebola West-Afrika verwoestte, produceerde een team van wetenschappers van de Wereldgezondheidsorganisatie en het Guinese ministerie van Volksgezondheid een vaccin dat 100 procent van de ontvangers tegen de infectie beschermde. En meer dan een dozijn bedrijven racen nu om een vaccin tegen het Zika-virus te produceren, dat in 2015 Zuid-Amerika binnenviel; een versie zou volgend jaar op de markt kunnen komen. Deze inspanningen waren monumentaal. Maar ze kunnen niet worden vergeleken met de zoektocht naar een universeel griepvaccin.
Het probleem is dat griep niet zoals andere ziekten is. Het is niet altijd zo dodelijk als ebola; het is niet zo nieuw als Zika. Het is een ziekte die zo bekend is dat we hem gebruiken als een synecdoche voor andere ziekten - we blijven thuis met 'een griep' die eigenlijk een verkoudheid is, of worden geveld door een 'maaggriep' die eigenlijk een gastro-intestinale bug is. En griep wordt veroorzaakt door een virus dat zo van vorm verandert dat we nooit hebben kunnen anticiperen op welke vorm het de volgende keer zal aannemen. De moeilijkheid van het nastreven van een universeel vaccin tegen griep is niet alleen de uitdaging om nieuwe wetenschap te maken. Het is de uitdaging om onze relatie te herleven met een ziekteverwekker die zo dicht bij ons staat dat we het niet duidelijk kunnen zien.

Abonneer je nu op het Smithsonian magazine voor slechts $ 12
Dit artikel is een selectie uit het novembernummer van Smithsonian magazine
Kopen














